
cGAS-STING信号通路在先天免疫、炎症、癌症及神经退行性疾病中发挥着重要作用。cGAS能够识别细胞内的双链DNA,并催化合成cGAMP;作为一种第二信使,cGAMP可激活STING。与cGAMP结合之后,STING便会发生寡聚化,并从内质网转运至高尔基体;这一转运过程是由COPII囊泡介导的。在高尔基体上,STING招募TBK1;TBK1随后对STING进行磷酸化修饰,进而招募IRF3并激活I型干扰素信号通路。STING内质网输出对于激活cGAS-STING信号通路的所有下游活动至关重要,然而,介导这一过程的分子机制目前尚不明确。
2026年3月25日,美国西南医学中心闫楠团队在Cell上发表了文章STING signaling modulation by COPII cargo recognition,揭示了STING内质网输出机制。

COPII囊泡中负责识别货物分子的是SEC24家族蛋白。哺乳动物表达四种SEC24同源蛋白,分别是SEC24A/B/C/D, 它们通过货物分子上的内质网输出基序(ERExitMotif)识别并转运货物分子。研究人员分别敲除每个SEC24同源蛋白,发现只有SEC24C敲除后显著降低STING活化。之后研究人员使用 AlphaFold3预测STING-SEC24C的结构,发现STING 338EEVTV343与SEC24C895LIL897相互作用。结合位点氨基酸突变均会减弱STING-SEC24C直接相互作用,进而抑制STING转运到高尔基体。序列比对显示,E339 和 E340 在大多数脊椎动物物种中是保守的;位于341和343位的氨基酸保守性较低,但均为疏水性氨基酸,因此研究人员将STINGER Exit motif 记作“EEΦxΦ” (x代表任意氨基酸,Φ代表疏水性氨基酸)。
和其他已知的SEC24C货物分子相比,STING和SEC24C的相互作用很弱,所以需要结合cGAMP形成寡聚化,招募更多的SEC24C后才能成功地转运到高尔基体。研究人员将STING内质网输出基序替换为亲和力更强的基序,设计出“super-ER-Exit”STING。这种STING突变体不需要结合cGAMP,也不需要形成寡聚化,便能自发转位到高尔基体上并激活下游通路。“Super-ER-Exit”STING在MC38肿瘤细胞中表达,诱导细胞凋亡并抑制肿瘤细胞增殖。在荷瘤小鼠实验中,这种STING突变体的表达显著抑制肿瘤生长并延长小鼠存活时间,显示出良好的抗肿瘤效果。
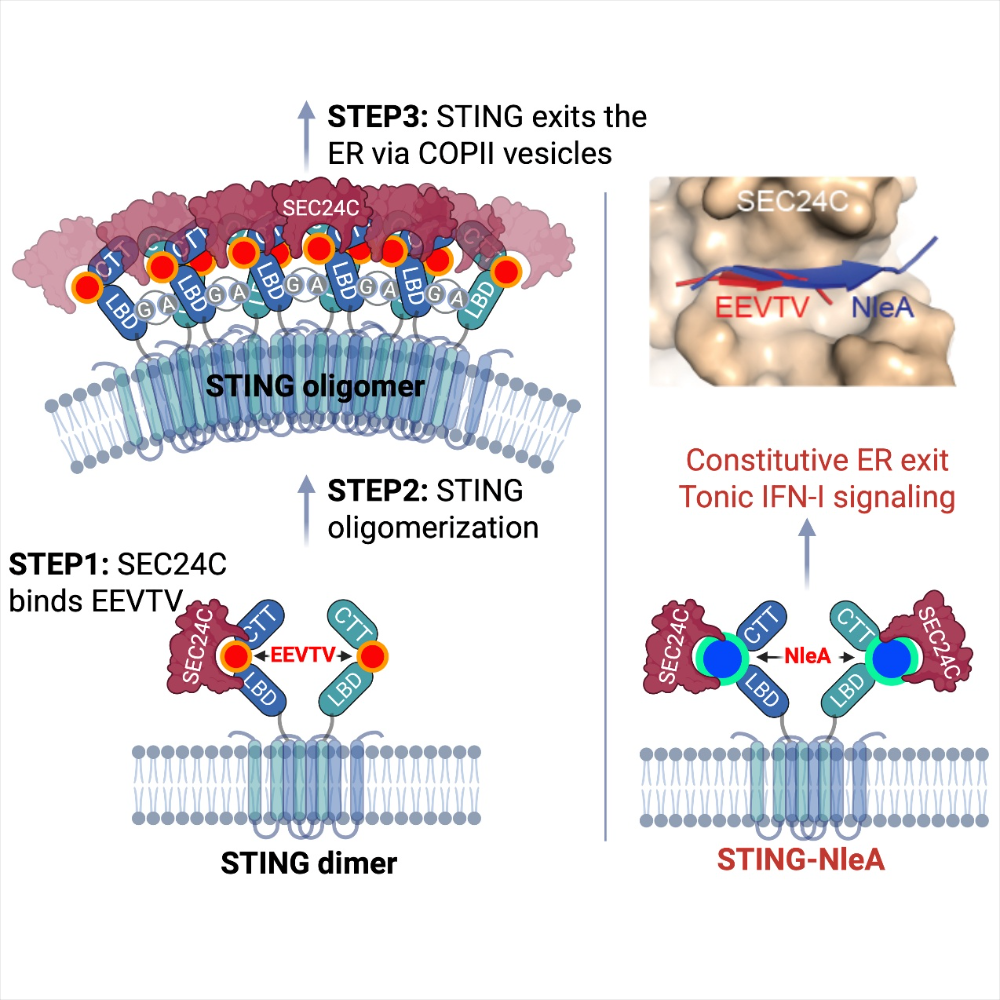
总之,本研究阐明了STING内质网输出机制,并提出了调控 STING 信号转导的策略。该过程或可作为靶点,来干预STING过度活化引起的自身免疫疾病。
闫楠组博士后吕恒为论文第一作者,博士后怀婉婉、宋琨、张慧(张学武组)以及博士生邢聪、Devon参与了本项研究。西南医学中心张学武老师在研究中提供了宝贵意见。